
알츠하이머 발병 메커니즘에 대한 연구가 지속되는 가운데, 일부 바이러스 감염이 영향을 줄 수 있다는 내용의 연구들도 주목을 받고 있다. 이 와중에 국내 연구팀이 새로운 치료 후보물질을 활용해, 알츠하이머와 바이러스 감염 사이의 연결고리를 입증하고 끊어내는 데 성공했다.
알츠하이머와 바이러스 감염의 연관성
알츠하이머는 전체 치매 중 약 60~70%를 차지하는 유형으로, 여러 종류의 치매 중 가장 흔하다. 일반적으로 알츠하이머는 ‘아밀로이드 베타 단백질’과 ‘타우 단백질’이 축적돼 발생하는 것으로 알려졌지만, 최근 이와 다른 접근법으로 발생 메커니즘을 연구하는 움직임이 늘어나고 있다.
그중 최근 연구에서는 신경계에 영향을 미치는 바이러스로 인해 알츠하이머와 같은 퇴행성 뇌질환이 발병할 수 있다는 결과를 내놓기도 한다. 신경계 염증이 알츠하이머의 유발 및 진행의 원인이라는 연구도 있었고, 대상포진 백신을 접종한 노인들에게서 치매 발병 건수가 줄었다는 연구도 발표된 바 있다.
또한, HSV-1(단순 헤르페스 바이러스 1형)으로 인해 발병할 수 있다는 연구도 있었다. 그러나 알츠하이머와 바이러스 감염이 어떤 관련이 있는지, HSV-1 감염이 퇴행생 뇌질환을 어떻게 가속시키는지에 대해서는 명확히 규명된 바가 없다.
고려대학교 의과대학 융합의학교실 신옥 교수는 동 대학 오수진 박사와 동아대학교 의과대학 윤진호 교수와 함께 연구팀을 구성해 알츠하이머와 바이러스 감염 사이의 연관성을 밝혔다. 이와 함께 신약 후보물질인 ‘ALT001’을 활용해 둘 사이의 연결을 차단하는 데 성공했다.
HSV-1 감염, 알츠하이머 가속화 입증
연구팀은 먼저 HSV-1 감염으로 인해 뇌의 면역세포인 ‘미세아교세포’ 기능에 영향이 있는지를 분석했다. ▲생쥐와 인간 유래 미세아교세포 ▲미세아교세포-신경세포 공배양 모델 ▲뇌 오가노이드 등 다양한 시스템을 활용했다.
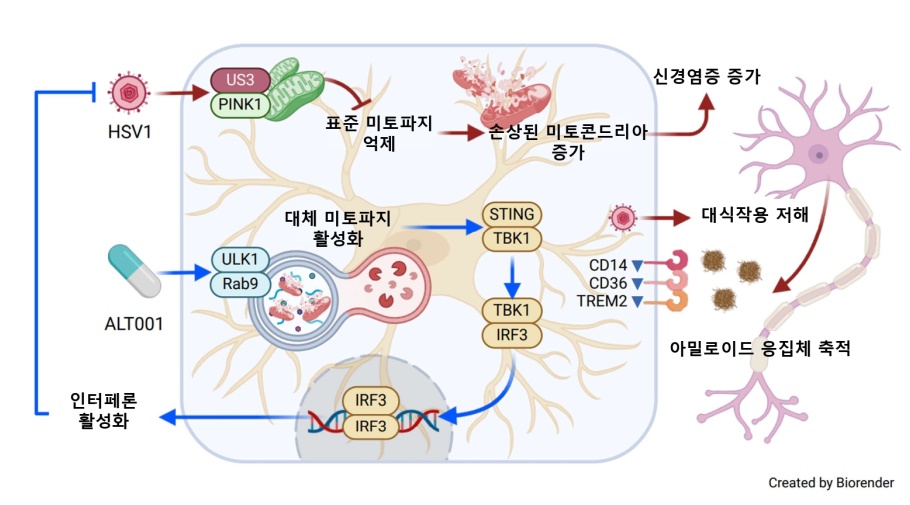
분석 결과, HSV-1 감염이 세포 내에서 손상된 미토콘드리아를 선택적으로 제거하는 과정인 ‘미토파지(Mitophagy)’를 방해한다는 것을 확인했다. 손상된 미토콘드리아 제거가 방해를 받으면서, 세포 전체에 걸쳐 미토콘드리아 기능이 저하된다는 것이다.
또한, HSV-1 감염은 아밀로이드 플라크와 같은 단백질 응집체를 제거하기 위한 식세포작용을 방해한다는 것도 확인됐다. 아밀로이드 플라크는 기존까지 알츠하이머의 주된 원인으로 알려져 왔다. 즉, HSV-1 감염이 퇴행성 뇌질환을 가속화할 수 있음이 입증된 것이다.
바이러스 억제로 신경계 퇴행 치료
연구팀은 이러한 실험 결과를 토대로, 자체 개발한 미토파지 촉진제 ‘ALT001’의 효과를 확인했다. ALT001을 통해 HSV-1 감염을 억제하고, 신경계에 발생한 염증을 완화할 수 있었다. 또한, 바이러스에 감염된 미세아교세포의 미토파지 기능을 정상화하는 것도 확인했다. 알츠하이머와 바이러스 감염 사이의 연관성을 입증한 한편, 회복 가능성까지 제시한 셈이다.
즉, ALT001을 활용해 바이러스 증식을 억제하는 한편, 신경계 염증 반응도 감소시켰다. 또한, 미세아교세포가 아밀로이드 플라크를 포함한 단백질 응집체를 더 잘 제거할 수 있도록 돕는다는 것도 확인됐다.
신옥 교수는 “이번 연구는 바이러스 감염이 알츠하이머를 포함한 퇴행성 뇌질환을 악화시킬 수 있다는 것을 분자 수준에서 입증한 동시에, 새로운 치료 전략을 제시했다는 점에서 의미가 크다”라고 이야기했다.
또한, 신 교수는 “특히 미세아교세포에서 HSV-1 감염이 미토파지에 미치는 영향을 규명한 것은, 기존 신경세포 중심 연구와는 차별화되는 성과로, ALT001은 향후 다양한 바이러스성 신경질환 치료에 적용할 수 있을 것”이라고 말했다.
이번 연구 결과는 국제 학술지 <테라노스틱스(Theranostics, IF=12.4)>에 게재됐다. 논문 제목은 ‘ALT001을 통한 미토파지의 약리학적 타겟팅이 단순포진 바이러스 1 매개 미세아교세포 염증을 개선하고 HSV1 감염을 제어하여 아밀로이드 베타 식세포작용을 촉진(Pharmacological targeting of mitophagy via ALT001 improves herpes simplex virus 1-mediated microglial inflammation and promotes amyloid beta phagocytosis by restricting HSV1 infection)’이다.
-
운동으로 분비되는 ‘엑서카인’, 알츠하이머 진행 완화
운동을 하면 근육에서 '엑서카인'이라는 물질이 분비된다. 이 물질이 신경계에 발생하는 염증을 완화할 수 있다는 연구 결과가 제기됐다. -
혈뇌장벽을 자연스럽게 통과하는 새로운 방법
뇌는 우리 몸에서 가장 중요한 기관이라 할 수 있다. ‘생명’을 유지하기 위한 중심기관이 심장이라면, 뇌는 ‘존재’를 유지하기 위한 중심기관이라 할 수 있다. 뇌는 우리 몸에서 가장 많은 에너지를 소비하는 기관이자, 여전히 풀리지 않은 비밀을 간직하고 있는 기관이기도 하다.높은 중요성으로 인해, 뇌는 스스로 보호할 수 있는 시스템을 여럿 가지고 있다. 가장 대표적인 것이 바로 혈뇌장벽(Blood-Brain Barrier, BBB)이다. 혈뇌장벽은 혈관과 뇌 사이에 존재하는 장벽으로, 뇌를 보호하기 위한 자연 보호막이라 할 수 있다. -
알츠하이머 치료제 후보 물질, 신경계 염증 줄이고 신경세포 보호
스페인 바르셀로나 대학의 한 연구팀이 최근 '신경계 염증'에 주목한 접근법으로 알츠하이머 치료제 후보 물질을 개발해 발표했다. -
머리 부상으로 ‘잠복 바이러스’ 활성화, 신경 퇴행 위험 높여
머리 부상을 자주 당하면 신경 퇴행성 질환에 걸릴 위험이 높아진다는 연구 결과가 제기됐다. -
자체 산소 생성 바이오잉크로 대규모 손상 근육 살린다
‘체적 근육 손실(VML)’은 대규모 외상으로 인해 골격근의 20% 이상 손실이 발생하는 경우를 말한다. 부산대, 인천대 공동연구팀이 VML 치료를 위한 자체 산소 생성 바이오잉크(bioink) 개발에 성공했다고 밝혔다. -
조류독감 백신 신규 개발, 동물실험으로 효과 입증
최근 우리나라에서도 조류독감에 관한 뉴스가 다뤄지고 있으며, 변종 바이러스가 포유류에게도 감염을 일으킨다는 사실이 알려지면서 인간 감염에 대한 위기의식도 대두되고 있다. 미국에서 개발 중인 조류독감 백신이 동물 모델을 상대로 뛰어난 효능을 보인 것으로 알려졌다. -
알츠하이머 조기 진단, 혈액 속 유전자 변화로 가능할 것
국내 연구팀이 혈액 검사를 통해 알츠하이머 조기 진단이 가능할 수 있다는 연구 결과를 제시했다. 혈액 속에서 알츠하이머 진행과 밀접한 유전자 발현 변화가 일어난다는 것을 밝혀낸 것이다. -
프리온 질환, 치명률 100% 극복하는 길 열었다
프리온 질환은 희귀 난치성 질환으로, 현재까지는 치료가 불가능해 ‘치명률 100%’로 알려져왔다. 최근 전북대학교 연구팀이 이에 대한 치료 가능성을 제시해 눈길을 끌고 있다. -
대상포진 백신 접종, 심혈관 질환 발생 위험 23% 낮춰
대상포진 백신 접종자의 경우 전반적인 심혈관 질환 발생 위험이 23% 가량 낮은 것으로 나타났다. 이는 뇌졸중, 심부전, 관상동맥 질환 등 다양한 심혈관계 질환을 모두 포함한 결과다. -
청력 손실과 치매, 중년 이후 청력 건강에 주의해야
청력 손실과 치매 사이에 연관성이 발견됐다는 내용의 논문이 발표됐다. 이는 평상시 청력 저하 위험이 있는지 살펴보고, 청력 건강에 더 관심을 기울여야 한다는 메시지를 던진다. -
헤르페스 바이러스, 알츠하이머 발병 위험과 관계 있어
입 주위에 포진이 생기는 ‘헤르페스’는 비교적 흔한 바이러스다. 그리 심각하게 여기지 않는 경향이 있지만, 최근 영국 의학 저널에 발표된 연구 결과를 보면 알츠하이머와 연관성이 있다는 근거가 제시됐다.

